欧洲药典(EP)在线查询攻略:3分钟掌握官方数据库使用技巧
欧洲药典(European Pharmacopoeia, Ph. Eur.)是原料药和制剂出口欧盟的黄金标准,其在线数据库EDQM官网是查询专论、对照品、法规更新的核心工具。本文提供一步步截图指导,助您高效获取关键信息,规避合规风险。

一、访问入口与账号注册
1. 官网地址
✅ 欧洲药典在线版:https://pheur.edqm.eu/
(注:免费账户仅可浏览专论目录,下载全文需订阅)
2. 账号注册
步骤:
1.点击右上角 “Login/Register” → “Create an account”;
2.填写机构邮箱、设置密码(建议企业邮箱);
3.激活邮件后完成注册(免费账户权限有限)。
订阅建议:
企业用户购买 “Online Access” 套餐,可下载PDF全文。
二、核心功能使用指南
1. 查询原料药专论(Monograph)
场景:确认某原料药(如阿莫西林)的EP标准。
操作步骤:
1.首页点击 “Search” → “Monographs”;
2.输入原料药英文名(Amoxicillin)或EP编号(*01/2008:0153*);
3.点击结果中的 “View PDF”(订阅用户可下载)。
专论关键内容:
Definition:化学结构与分子式;
Characters:性状、溶解度;
Tests:有关物质、残留溶剂、重金属等检测方法;
Assay:含量测定方法;
Storage:储存条件。
2. 获取对照品信息(Reference Standards)
场景:订购阿莫西林EP对照品(批号Y0000000)。
操作步骤:
1.首页点击 “Reference Standards” → “Catalogue”;
2.搜索 Amoxicillin → 查看库存状态(Available/Low Stock);
3.记录 “Order Code”(如 Y0000000),点击 “Order” 跳转采购页。
注意:
1.对照品需通过 EDQM官方商店购买(https://shop.edqm.eu/);
2.中国用户推荐选择 “DHL Express” 物流(3-5工作日达)。
3. 查询通则(General Chapters)
场景:确认残留溶剂(EP 5.4)或无菌检测(EP 2.6.1)方法。
操作步骤:
1.首页点击 “General Texts” → “General Chapters”;
2.按章节号(如 *5.4*)或关键词(Residual Solvents)搜索;
3.下载PDF查看详细方法。
重点章节:
<2.2.46> :气相色谱法(残留溶剂检测);
<2.6.1> :无菌检测法;
<5.10> :基因毒性杂质控制策略。
三、高级功能:法规追踪与更新提醒
1. 药典版本与增补本查询
当前版本:EP 11.6(2023年7月生效);
查看路径:首页 → “About Ph. Eur.” → “Current Edition”。
2. 专论更新订阅
操作步骤:
1.登录账号 → 进入目标专论页面(如 Insulin);
2.点击 “Subscribe to Alerts” → 勾选 “Monograph updates”;
3.更新时自动邮件通知(含修订内容对比)。
四、免费替代方案(非订阅用户)
1. 有限预览功能
未订阅用户可在专论页面点击 “Preview”,查看前两页内容(含定义与性状)。
2. 各国药监局官网
德国BfArM:部分公开EP专论(德语版);
法国ANSM:提供关键章节摘要。
3. 第三方数据库
Pharmacompass:免费检索专论目录与更新日期(无全文);
DrugFuture:中国药典与EP对照查询(部分翻译)。
五、常见问题与解决技巧
1. 专论查不到?
可能原因:
❌ 名称拼写错误(如 Paracetamol 非 Acetaminophen);
❌ 该品种无EP专论(需走ASMF路径)。
解决:改用 CAS号(103-90-2) 或 通用名检索。
2. 对照品缺货?
应对策略:
联系EDQM客服获取预计到货时间;
临时使用 USP/ChP对照品(需进行方法学比对)。
3. 新旧版本冲突?
案例:EP 10.0与EP 11.6对某杂质限度要求不同。
原则:以产品上市时生效版本为准(过渡期通常6个月)。
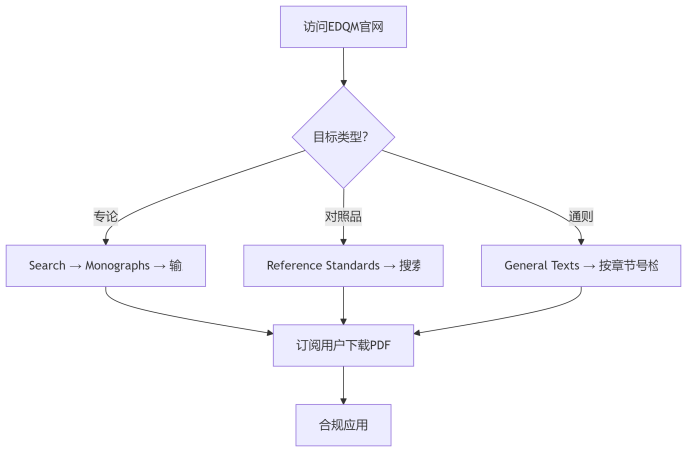
六、总结:高效查询流程图