美国FDA认证全球数据库(GUDID)和设备标识符(UDI)
FDA认证已经建立了独特的设备识别系统,可以通过在医院中分发和使用医疗设备以及其他实践来识别医疗设备。通过这种通用系统,大多数设备的标签都应包含人类和机器可读格式的唯一设备标识符(UDI)。FDA还要求医疗设备标签商向FDA的全球唯一设备标识数据库(GUDID)提交有关每种设备(包括UDI)的某些信息。
商通检测可以帮助您确定您的设备是否需要FDA的UDI以及将您的设备信息提交到FDA的全球唯一设备标识数据库(GUDID)。
商通检测提供美国FDA认证服务!
什么是UDI?
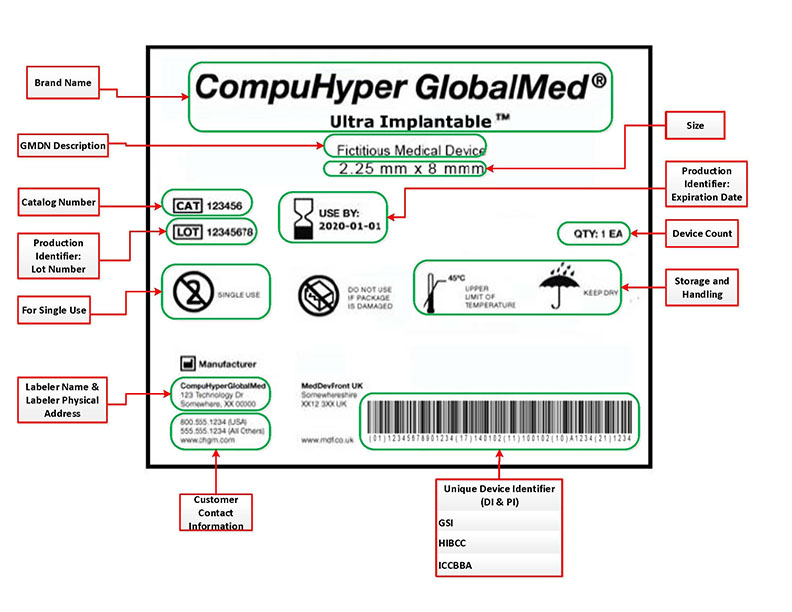
唯一设备识别(UDI)系统旨在通过分发和使用来提供全球统一的医疗设备正面肯定标识,要求设备标签带有全球唯一的设备标识符(通过使用“自动识别和数据捕获”来传达) (如果适用,则基于标准的“人类可读解释”),该唯一标识符的UDI-DI(设备标识符)也链接到特定于辖区的公共UDI数据库(来源:国际医疗器械监管者论坛(IMDRF):http ://www.imdrf.org/)。
在美国食品和药物管理局(FDA) ,在欧盟委员会和其他监管机构已通过制定UDI的规定使得患者安全的战略重点医疗器械和体外诊断(IVD)设备,并要针对对准全球统一和一致的方法关于IMDRF指南。
美国食品药品监督管理局(FDA)在2013年9月发布了一项UDI规则,该规则建立了适用于投放到美国市场的所有医疗设备的UDI系统。
2013年12月17日,GS1已获美国FDA认可为唯一设备标识符(UDI)的发行机构。GS1标准符合美国FDA发行UDI的标准。全球GS1成员组织将帮助制造商按照美国FDA UDI法规的要求实施,以支持患者安全和供应链安全。
管制产品数据必须提交到全球唯一设备识别数据库(GUDID),即美国FDA UDI管制数据库。










