中国dmf备案是什么?
中国dmf备案是什么?
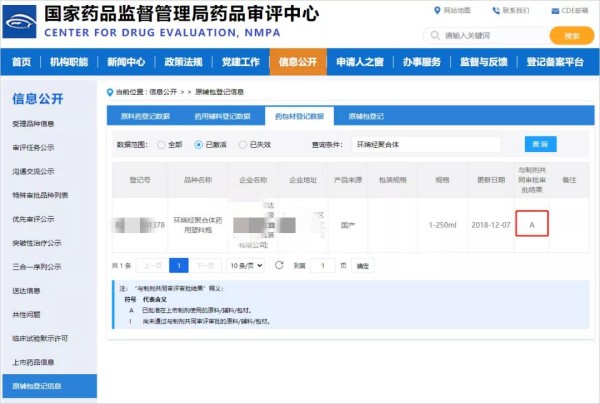
中国DMF备案是指在中国,所有的原料药(除了创新药物的原料药)、辅料(除了豁免清单)和包装材料需要在中国药品审评中心(CDE)注册,并公布在CDE网站上的过程。
在中国,药品主文件(DMF)的备案管理相较于美国FDA的药品主文件(DMF)更为严格。FDA的DMF是自愿提交的信息,旨在提供人类药品生产、加工、包装和储存过程中使用的设施、工艺或物品的详细机密信息,而制造商向FDA提交这些信息并非强制性。
然而,在中国,除了创新药物的原料药外,所有的原料药、辅料和包装材料都需要在CDE进行注册,并且相关信息需要公布在CDE网站上。这种做法与美国FDA的自愿性DMF提交形成了鲜明对比,体现了中国在药品备案管理上的严格性和透明度要求。
在中美双报的情况下,DMF(Drug Master File)的具体差异包括费用、文件内容和审查程序等方面。这意味着,对于那些需要在中美两国同时申请药品的企业来说,需要了解并遵守两国不同的DMF备案要求和程序,以确保其药品申请能够顺利通过两国的审查。
中国DMF和美国DMF申报有什么区别?
中国DMF(Drug Master File)和美国DMF(Drug Master File)虽然名称相同,但是在申报和使用上有一些区别。
1. 中国DMF:
- 中国DMF是在中国国家药品监督管理局(NMPA)管理下的药品主文件。它是一种包含特定药品制造工艺、控制方法、质量数据和稳定性数据等详细信息的文件。
- 中国DMF通常由药品原料供应商、药品包装材料供应商或者制药工艺的提供者提交给NMPA。这些信息对于药品的注册审批或GMP(Good Manufacturing Practice,良好生产规范)认证是必需的。
2. 美国DMF:
- 美国DMF是由美国FDA管理的药品主文件。它包含了与药品生产相关的详细信息,例如药品的化学、制造、控制、稳定性数据以及其它支持文件。
- 美国DMF通常由药品原料供应商、包装材料供应商或者制药工艺的提供者提交给FDA。这些信息可以作为申请新药批准(NDA)、通用药物申请(ANDA)或生物等效性评价(BE)的支持文件。
区别和关系:
- 审批机构不同:中国DMF提交给NMPA,而美国DMF提交给FDA。
- 使用范围略有不同:虽然都是为了支持药品的生产和注册,但具体的法律法规、审批流程和使用要求可能有所不同。
- 信息要求和标准:尽管目的相似,但具体的信息内容和格式可能因国家的法规和行业实践有所不同。
美国DMF申报一般比中国DMF申报周期快一些。
商通检测为:原料药、化学药品、生物制品提供专业GMP合规咨询服务和相关注册办理,助力各类医药企业建立或完善符合中国、美国、欧盟、日本等药品质量体系。
从现场考查、现状评估环节结合企业实际确定项目方案,以注册资料、GMP法规及指南为标准,指导和带领企业进行生产现场GMP“软”“硬”件的整改与完善,帮助企业全面做好“GMP符合性检查”前的各项准备工作,通过GMP现场检查。










