响应FDA认证483检查意见的7个步骤
注意:如果您是一家医疗器械公司,并且拥有在FDA认证注册的II类或III类产品,则将接受FDA认证的检查。
无论您之前是否已经通过FDA认证检查,我强烈建议您花一些时间为即将来临的访问做准备。
有一些方法会使您的FDA认证检查失败,并收到数十个FDA认证 483检查意见。尽管您已尽力而为,但很有可能会收到一些483。
您在FDA认证的检查过程中的行为是很重要的,当然。但是,与FDA认证相对应的检查后行为以及关闭483s更为重要。
在FDA认证检查员完成检查时,他将与您分享其观察结果的摘要。如果检查员发现问题,他将讨论并提供FDA认证 483号检查意见表。检查员将询问您是否同意更正问题并记录您的答复。
并且,请确保您了解FDA认证检查员的观察和评论。在检查员完成483草稿并离开您的设备之前,请先提问。清楚地了解问题对于您能够解决并满足FDA认证的关注非常重要。
接下来的工作是朝着483s分辨率努力的最重要步骤。意识到时钟在滴答作响,您有15天的时间就483个观察结果向FDA认证做出初步答复。

FDA认证 483检查应对步骤:
步骤1:建立响应活动的时间表
FDA认证检查完成后,您会收到483个观察结果的列表,时钟开始计时。您现在有15天的时间对FDA认证做出回应。
我强烈建议您在减轻FDA认证问题方面的第一步是为准备响应制定牢固而积极的时间表。即使您只有483个,这15天的飞行时间也会非常快。
您希望最初的反应是彻底的,并代表您对纠正检查员发现的所有问题的承诺。以下概述的步骤应作为主要步骤的指南,以包括在此响应时间表中。意识到您的483响应是一个项目。那样对待。
步骤2:找出根本原因
手上有483个观察值,您需要确定问题的根本原因。根本原因分析可能是您整个CAPA程序的一部分。有许多用于分析根本原因的工具和技术,例如鱼骨图和5个Whys。
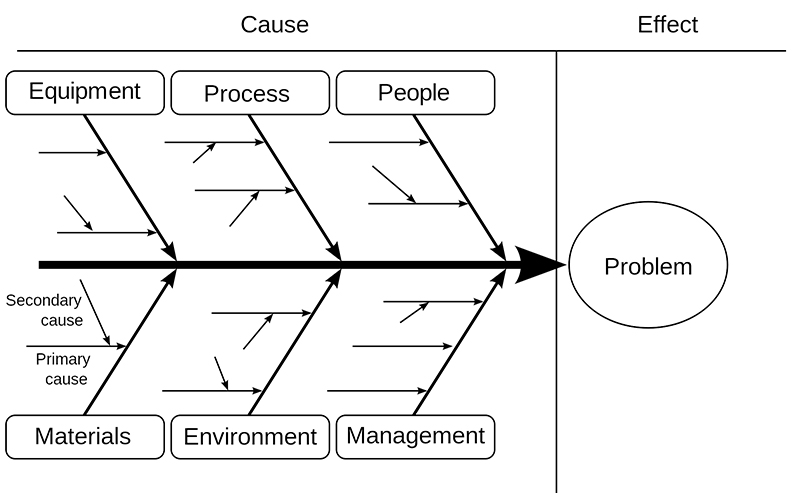
只要您找到真正的根本原因,工具的选择就不太重要。确定根本原因的一个非常常见的错误是,这通常是问题或问题的重述。
步骤3:签发CAPA
一旦为每483次观察确定了根本原因,就应起草并发布纠正措施计划或CAPA。我建议您为每个单独的483发出单独的CAPA。
您的CAPA应指定:
1.问题说明,复制并粘贴FDA认证 483观察结果的准确措辞
2.根本原因分析
3.需要立即更正
4.纠正措施计划,以防止发生/再次发生
5.CAPA所有者的分配
步骤4:建立处理483S的时间表
FDA认证希望您能紧急解决并缓解这些问题。在制定CAPA和特定的行动计划时,还应建立时间表。CAPA是项目,应采用良好的项目管理规范。
您可能要超级进取,并承诺尽快解决483。不要陷入这个陷阱!您的下意识反应是在提交您的初始响应之前,尝试解决所有问题。
FDA认证希望您遵循CAPA程序,并花费适当的时间来纠正问题并防止这些问题再次发生。是的,这些CAPA可能会成为公司首要任务。只是现实一点。
步骤5:草拟初次回应函
既然您已经知道需要什么(至少从较高的层次上来说),现在该起草您的第483个答复信以发送给FDA认证了。
我建议包括一个附录(如上一封信中所述),该附录总结了每个单独的483观察以及解决所需要的纠正措施。您可以包括CAPA的副本。
步骤6:一致的跟进
在您的初始回复信中,您应指定何时将下一次更新提供给FDA认证,以及发送更新的频率。在某种程度上,这将取决于所需的校正量。根据经验,我建议每4-6周发送一次更新。
对于每个后续的更新信函,您应该非常重复。这封信的主体可能与最初的回复非常相似。您应该始终包括附录,说明初次答复中提供的相同信息,同时包括有关项目完成时间的更新。
FDA认证可能会对每个信件做出回应。
当您认为您已经成功处理了483个观察结果时,那么您下一次与FDA认证的往来信件应注明。FDA认证可能会做出回应,并可能有后续问题或接受您的声明。
步骤7:准备好进行重新检查
是的,是的。一旦您成功完成对483个观察值的校正,很有可能您将得到FDA认证检查员的随访。下次访问可能会被宣布。
后续行动的目的是验证您的公司已解决并记录了已采取的适当措施,并观察到纠正措施得到有效实施。通常,此后续检查仅需几天,除非FDA认证检查员不满意。
fda认证问题可咨询商通检测!










